
Во всем мире для диагностики эндотоксинов на смену лизатам амебоцитов животного происхождения приходят рекомбинантные реактивы. Такая практика – без использования животных – это прорыв в исследованиях, а теперь ее преимущества могут ощутить и украинские фармпроизводители, благодаря ООО «Химлаборреактив». ХЛР является официальным дистрибьютором Associates of Cape Cod, Inc. – пионера и уже 50 лет глобального лидера в производстве продуктов и сервисов для определения бактериальных эндотоксинов и бета-глюканов. В своей статье научные сотрудники ГП «Український науковий фармакопейний центр якості лікарських засобів» (Харьков) и специалисты компании ХЛР рассказывают об особенностях и преимуществах новейших реактивов.
Фармакопейное испытание лекарственных средств и медицинских изделий на бактериальные эндотоксины в тесте in vitro официально признано в 1980 году, когда его впервые включили в Фармакопею США 20-го издания. Основой для метода анализа бактериальных эндотоксинов стала открытая Фредериком Б. Бенгом (F. B. Bang) и Джеком Левином (J. Levin) реакция свертывания крови у древнейших представителей типа членистоногих из ныне существующих – мечехвостов (Limulus polyphemus).
Сохранить популяцию реликтовых животных
Ежегодно в водах Атлантики вылавливают примерно 6000 мечехвостов для производства реактива, что очень вредит популяции реликтового вида. Осознавая это, компания Associates of Cape Cod Inc. (США), ведущий производитель реактивов для тестов на бактериальные эндотоксины, разработала новые реактивы из рекомбинантного белка вместо лизата животного происхождения.
При использовании любого натурального ингредиента возникает значительная вариабельность чувствительности природного лизата. Ее могут вызывать пол, возраст, размер мечехвостов, особенности конкретной среды их жизни, сезон и время забора гемолимфы, а также активность ферментной системы лизата, выраженность которой генетически детерминирована. Естественный лизат содержит и ряд других белков, по меньшей мере десять из них участвуют в антимикробном ответе и могут либо препятствовать, либо усиливать его коагуляционную активность.
Каждый поставщик получает и очищает лизат особым способом: экстрагирует составляющие хлороформом, оставляет в лиофилизате денатурированные белки, добавляет буферные растворы и детергенты – дополнительный источник изменчивости. Все это влияет на чувствительность полученного реактива к бактериальным эндотоксинам и часто приводит к значительным различиям в результатах анализа лекарственных средств. Поэтому существует мнение, что рекомбинантные белки более стабильны, а значит, можно получать сопоставимые результаты испытаний.
Лизат биологического происхождения имеет еще один недостаток – наличие в гемоцитах лизата альтернативного механизма активации процессов гелеобразования через глюкан-чувствительный фактор G (путь фактора G). Десять лет лизат амебоцитов Limulus использовали для контроля фармацевтической продукции, а затем случилось потрясающее открытие – способность других материалов, а именно (1,3)-β-D-глюканов, являющихся компонентом клеточных стенок дрожжевых и других грибов, вызывать ложноположительную реакцию, когда бактериальных эндотоксинов в препарате мало или вообще отсутствуют.
Достижения генной инженерии и дальнейшее коммерческое производство
Коагуляционная система мечехвостов уже давно является объектом усилий для специалистов по генной инженерии. Супруги-ученые из Национального университета Сингапура – Динг Джик Линг (Ding Jeak Ling) и Хо Боу (Ho Bow) – поняли, какой огромный потенциал имеет синтезированный в лабораторных условиях рекомбинантный фактор С для разработки технологии выявления эндотоксинов без использования животных. В 1995 году они клонировали полноразмерный фактор С, а в 1997-м клонировали и экспрессировали рекомбинантный фактор С (rFC) у разных хозяев. Благодаря исследованиям ученые смогли установить, что при одинаковых условиях анализа rFC имеет более низкие фоновые показатели и более чувствительный ответ на эндотоксин по сравнению с использованием коммерческого ЛАЛ-реактива.
Переход к коммерческому производству рекомбинантных реактивов ознаменовал новейшую эпоху в количественной диагностике эндотоксинов. Первый коммерческий реактив на основе рекомбинантного фактора С для микрофлуорометрического анализа эндотоксинов был предложен в 2004 году, позже появились другие разработки. А в апреле 2021 года Associates of Cape Cod., Inc. (США) совместно с японской компанией Seikagaku Corporation ввела в линейку коммерческих предложений рекомбинантный каскадный реактив (rCR) PyroSmart NextGen™, клонированный из генов Limulus polyphemus, который, подобно коагуляционной системе мечехвоста, содержит все ферменты процесса коагуляции – факторы В и С и свертывающий фермент вместе с хромогенным субстратом, но исключает β-глюкан-специфический белок фактора G.
Рекомбинантный реактив PyroSmart NextGen® позволяет количественно выявлять бактериальные эндотоксины с помощью хромогенного кинетического метода, который является дальнейшей эволюцией гель-тромб- и турбидиметрических тестов. Хромогенный метод основывается на количественной зависимости, которую имеет интенсивность окраски реакционной смеси от концентрации эндотоксинов: большее содержание эндотоксина способствует тому, что фермент быстрее расщепляет субстрат – но не коагулоген, как в природе, а хромогенный пара-нитроанилин (pNA), это дает насыщенный желтый цвет (табл. 1).
Таблица 1. Сравнительный анализ хромогенного кинетического метода с PyroSmart NextGen® и лизатом амебоцитов
| Показатель и характеристика | PyroSmart NextGen™ | Лизат амебоцитов Limulus |
| Оборудование | Инкубационный мікропланшетний ридер, например, BioTek® ELx808™ | Ридер для пробирок или инкубационный микропланшетный ридер |
| Длина волны, нм | 405 нм / 490 (492)* | 405 |
| Программное обеспечение | Позволяет обрабатывать данные по времени начала достижения определенной оптической плотности или по скорости реакции, например, Gen5™, Pyros® eXpress | |
| Состав набора | Реагент и буферный раствор для восстановления (PyroSmart NextGen®Reagent / PyroSmart NextGen® Reconstitution Buffer) | Реагент и буферный раствор для восстановления |
| Условия хранения реактивов, ℃ | 5 ± 3 | |
| Состав реагента | Три рекомбинантных белка:
| Четыре рекомбинантных белка:
|
| Глюкан-блокировочный буферный раствор | Не применяется | Glucashield® buffer |
| Чувствительность метода, МО/мл | 0,005 | 0,001 |
| Микропланшеты | 96-луночные микропланшеты с крышкой, свободные от бактериальных эндотоксинов и глюканов | |
| Смешиваемые объемы мл | 0,05 | 0,05 / 0,1 |
| Температура реакции, ℃ | 37 ± 1 | |
| Время инкубации, мин | 30–60 | 60–90 |
| Интервалы считывания во время инкубации, с | 30* | 10–30 |
| Критерий пригодности (коэффициент корреляции стандартной кривой) | ≥ 0,98 | |
* – в зависимости от возможностей планшетного ридера.
Биотехнологическое производство PyroSmart NextGen® – это гарантия стабильного от партии к партии продукта, на чувствительность которого к эндотоксинам не влияет изменчивость природных белков. Высокое качество rCR подтверждают надежность и хорошая воспроизводимость критериев пригодности стандартной кривой и постоянство параметров реакции коагуляции.
Установлено, что PyroSmart NextGen® и лизат амебоцитов Limulus превосходят эффективность rFC к выявлению автохтонных эндотоксинов микрофлоры воды, поэтому являются самым распространенным сырьем на фармацевтическом предприятии.
Результаты экспериментов, проведенных компанией Associates of Cape Cod. Inc., свидетельствуют, что реактив PyroSmart NextGen® проявляет определенные преимущества при условиях тестирования интенсивно окрашенных растворов по сравнению с лизатами животного происхождения для хромогенного и турбидиметрического методов.
В исследовании, выполненном Масаши Мурои (М. Muroi) с коллегами в 2019 году, рекомбинантные реактивы PyroSmart и rFC и пять лизатов животного происхождения продемонстрировали при идентичных условиях анализа сравнимую реакционную способность к эндотоксинам 13 различных штаммов грамотрицательных бактерий. Кроме того, не только не было зафиксировано существенных отличий в результатах анализа 109 образцов парентеральных препаратов, а рекомбинантные реагенты даже характеризовались от серии к серии заметно более высокой воспроизводимостью результатов, чем лизаты амебоцитов. По мнению авторов, это достаточно убедительно демонстрирует, что рекомбинантные реагенты, в частности PyroSmart – очень надежный инструмент, равноценный или даже лучший, чем природный лизат амебоцитов, и пригодный для рутинных испытаний эндотоксинов на фармацевтическом предприятии.
 |  |  |
Метод, признанный мировыми фармакопеями
Анализ эндотоксинов с использованием рекомбинантных реактивов постепенно принимают ведущие фармакопеи мира. С 1 января 2021 года в Европейской Фармакопее вступила в силу общая статья «Test for bacterial endotoxins using recombinant factor C» (2.6.32) со ссылкой на флуорометрический метод определения эндотоксинов с рекомбинантным фактором С. В том же году в Фармакопее Японии была опубликована общая информация об использовании рекомбинантных реактивов (rCR) и (rFC) в качестве альтернативных тестов («Bacterial Endotoxins Test and Alternative Methods using Recombinant Protein-reagents for Endotoxin Assay »), где отмечено, что анализ эндотоксинов с некоторыми из рекомбинантных белковых реагентов проявляет одинаковую или лучшую чувствительность и специфичность, чем в методе с использованием реактивов лизата. Фармакопея США рассматривает эти методы как альтернативные в общей статье <86> «Bacterial endotoxins test using recombinant reagents», действующей с 1 мая 2025 года.
В собственных экспериментальных исследованиях мы оценивали аналитические характеристики (правильность, линейность, прецизионность, диапазон применения и пределы количественного определения) в соответствии с требованиями общей статьи «Валидация аналитических методик и испытаний» (5.3.N.2., ГФУ 2.4), Руководства ICH Q2 и USP <125.
Исследования проводились с использованием рекомбинантного реактива PyroSmart NextGen® и стандартного препарата эндотоксина CSE (Escherichia coli O113:H10), любезно предоставленных Associates of CAPE COD, Inc. (США) при посредничестве ООО «Химлаборреактив» (Украина). Для исследования применен хромогенный кинетический метод в режиме «Onset time assay» при длине волны 405 нм на микропланшетном ридере ELx808 производства компании BioTek Instruments Inc. (США). В качестве лизата амебоцитов использовали Pyrochrome® от Associates of CAPE COD, Inc.
Аналитические характеристики и критерии приемлемости испытания с использованием рекомбинантного реактива PyroSmart NextGen® приведены в табл. 2. Стандартные кривые для определения эндотоксинов, полученные с помощью PyroSmart NextGen®, удовлетворяли критерию надежности (r ≥ 0,980) и равнялись 0,998–1,0 (см. рисунок).
Таблица 2. Параметры регрессионного анализа содержания бактериальных эндотоксинов с PyroSmart NextGen® и лизатом амебоцитов
| Требование | Реактив / тест-набор | ||
| PyroSmart NextGen® | Лизат амебоцитов Limulus | Критерий приемлемости | |
| Линейность | |||
| Коэффициент корреляции ǀrǀ в диапазоне концентраций эндотоксинов, указанных изготовителем, МО/мл | ǀrǀ =1,00 (max) ǀrǀ = 0,998 (min) 0,005–50 | ǀrǀ = 1,00 (max) ǀrǀ = 0,993 (min) 0,005–5 | ǀrǀ ≥ 0,980 |
| Правильность | |||
| Концентрация добавленных эндотоксинов, МО/мл | Количество выявленных эндотоксинов, (min – max, %) | 50–200 % | |
| 0,005 0,05 0,5 5 50 | 100,0–120,0 90,0–96,0 90,4–110,6 85,4–97,9 98,8–1000 | 100,0–120,0 84,0–142,9 108,2–110,2 78,9–87,4 – | |
| Прецизионность – сходимость | |||
| Концентрация добавленных эндотоксинов, МО/мл | Коэффициент вариации (min CV – maxCV, %) | CV ≤ 25 % (0,005 МО/мл) CV ≤ 20 % (0,05–50 МО/мл) | |
| 0,005 0,05 0,5 5 50 | 15,63–24,08 13,41–20,64 6,82–21,22 4,87–8,53 – | 2,56 3,73–10,29 3,23–29,23 1,63–6,46 – | |
| Диапазон применения | |||
| 0,005 – 50 МО/мл | Удовлетворительные результаты исследований валидационных характеристик прецизионность, правильность и линейность свидетельствуют, что методика обеспечивает линейность, правильность и прецизионность в пределах исследованного диапазона применения. | ||
| Предел количественного определения | |||
| 0,005 МО/мл | Правильность: 100,0–120,0 % Прецизионность: 15,63–24,08 % | Удовлетворительные результаты исследований прецизионность и правильность для самой низкой концентрации | |
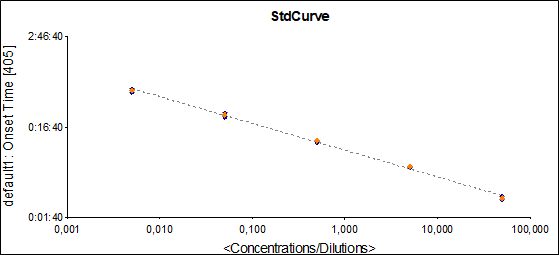
Рисунок. График зависимости сигнала как функции концентрации эндотоксинов
(стандартная кривая получена с помощью PyroSmart NextGen®).
Ось ординат (Y) – «время начала»; ось абсцисс (X) – «концентрация»
Визуальная оценка графика зависимости сигнала как функции концентрации эндотоксинов свидетельствует о наличии линейной зависимости (см. рисунок).
Как видно из табл. 2, восстановление добавленного эндотоксина в процентах от известной концентрации добавленных эндотоксинов удовлетворяет критерию приемлемости для проверки мешающих факторов, как описано в общей статье ГФУ 2.6.14, то есть 50–200 %. Диапазон составляет 0,005–50 МЕ/мл, нижний предел количественного определения – 0,005 МЕ/мл (см. табл. 2).
Краткие итоги
Подытоживая массив данных из научных публикаций, информационно-справочных материалов компании Associates of Cape Cod Inc., а также результаты собственных экспериментальных исследований, мы отметили ряд преимуществ, свойственных рекомбинантному реактиву (rCR) по сравнению с лизатом амебоцитов животного происхождения. Главные из них:
- Меньшая вариабельность реагента от партии к партии, что повышает внутрилабораторную сопоставимость результатов и воспроизводимость критериев пригодности стандартной кривой
- Исключение ложноположительных результатов через индифферентность к (1,3)-β-D-глюканам и (1→4)-β-D-глюканам)
- Более высокая реакционная способность к Helicobacter pylori GU2 в экспериментальных исследованиях с использованием PyroSmart NextGen®, чем у других рекомбинантных реагентов (rFC), и существенно более низкий мешающий уровень влияния кальция гепарина
- Выявление преимуществ при анализе интенсивно окрашенных растворов
- Содействие меньшему использованию животных в фармакопейном контроле в соответствии с положениями 3R Европейской конвенции
ХЛР, как официальный представитель компании Associates of Cape Cod в Украине, предлагает:
- Широкий ассортимент реактивов и систем для анализа содержания эндотоксинов
- Методическое сопровождение, консультации по подбору оптимального решения для любого препарата (специалисты компании ХЛР постоянно проходят обучение на базе мощностей производителя)
- Снабжение с соответствующими условиями перевозки и хранения на сертифицированном складе
Обращайтесь в компанию «Химлаборреактив», и вы получите лучшие решения для контроля качества в фармацевтической отрасли!
Татьяна Леонтьева,
научный сотрудник лаборатории фармакопейного анализа ГП «Український науковий фармакопейний центр якості лікарських засобів», Харьков
Юлия Меркулова,
канд. биол. наук, ведущий научный сотрудник лаборатории фармакопейного анализа ГП «Український науковий фармакопейний центр якості лікарських засобів», эксперт Европейской Фармакопеи
Анна Журба,
ведущий специалист Отдела химических реактивов компании ХЛР